Naturstoffsynthese
Im Laufe der Evolution hat die Natur eine große Vielfalt an Molekülen hervorgebracht, die die unterschiedlichsten Effekte bei Kontakt mit lebenden Organismen hervorrufen können. Einige Naturstoffe mit bestimmten biologischen Aktivitäten können Krankheiten oder Vergiftungen verursachen, andere hingegen in der Medizin – z. B. als Antibiotikum oder Schmerzmittel – genutzt werden. Insbesondere Pflanzen verschiedenster Art, Pilze und Bakterien produzieren Moleküle, die eine therapeutische Wirkung aufweisen und somit den Forschern in Medizin, Chemie und Pharmazie Anhaltspunkte geben, welche Struktur ein Molekül aufweisen sollte, um als Wirkstoffkandidat in Frage zu kommen.
Dazu müssen die entsprechenden Substanzen isoliert und ähnliche Verbindungen hergestellt werden, um deren Wirkmechanismus zu untersuchen. Zum Einsatz als Medikament werden allerdings so große Mengen der Naturstoffe benötigt, dass sie nur in den wenigsten Fällen direkt aus den sie produzierenden Organismen gewonnen werden können, sondern mit Hilfe der Biotechnologie/Gentechnik oder auch per „Totalsynthese" in einem chemischen Labor hergestellt werden müssen. Unter Totalsynthese versteht man den Aufbau eines komplexen Moleküls aus einfachen, in großen Mengen verfügbaren Substanzen.
Im Rahmen unserer Forschung auf dem Gebiet der organischen Chemie entwickeln wir synthetische Zugänge zu diversen biologisch aktiven Naturstoffen; zentrales Ziel hierbei ist die Entwicklung flexibler Synthesestrategien für die Herstellung dieser Naturstoffe und ihrer künstlichen Analoga. Totalsynthesen folgender Moleküle werden zur Zeit in unserem Arbeitskreis unter anderem entwickelt:
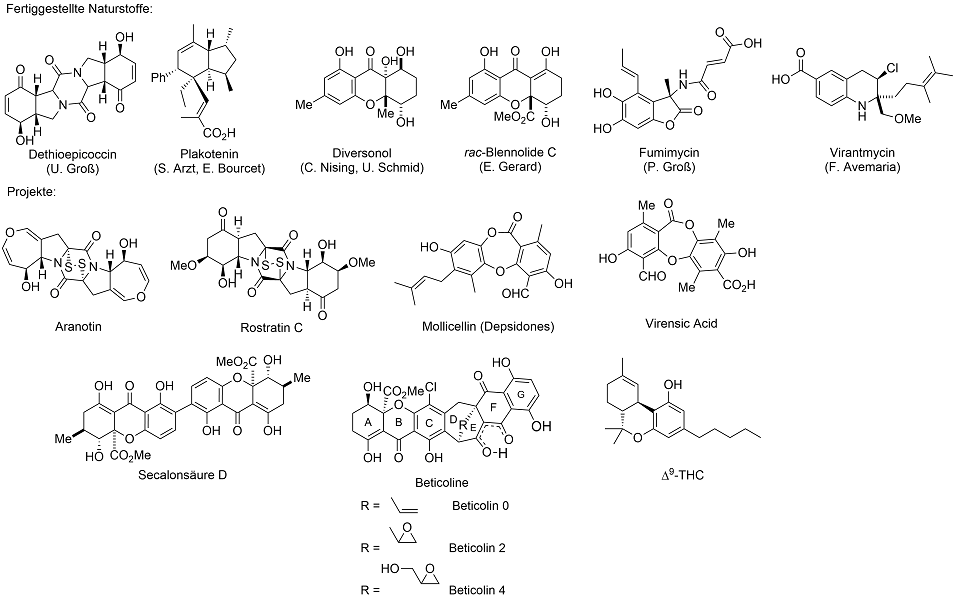
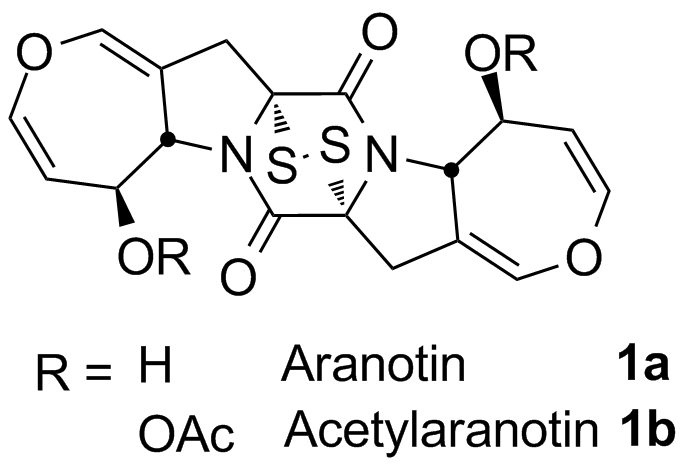
Aranotin
Beticolin 0
Mykotoxine sind Sekundärmetabolite aus Pilzen, die schädliche Auswirkungen auf Menschen, Tiere und Nutzpflanzen haben, was zu Krankheiten und wirtschaftlichem Schaden führt.
Beticoline sind Mykotoxine, die vom Pilz Cercospora beticola produziert werden, der für die Blattfleckenkrankheit verantwortlich ist und weltweit schwere Schäden an Nutzpflanzen verursacht. Darüber hinaus zeigten biologische Studien ein breites zytotoxisches Profil von Beticolinen. Um diesen Wirkmechanismus untersuchen zu können, sind wir daran interessiert, eine Syntheseroute zur Darstellung des hochkomplexen polyzyklischen Gerüsts dieser Naturstoffe mit einem einzigartigen Bicyclo[3.2.2]nonan-Ringsystem zu entwickeln.
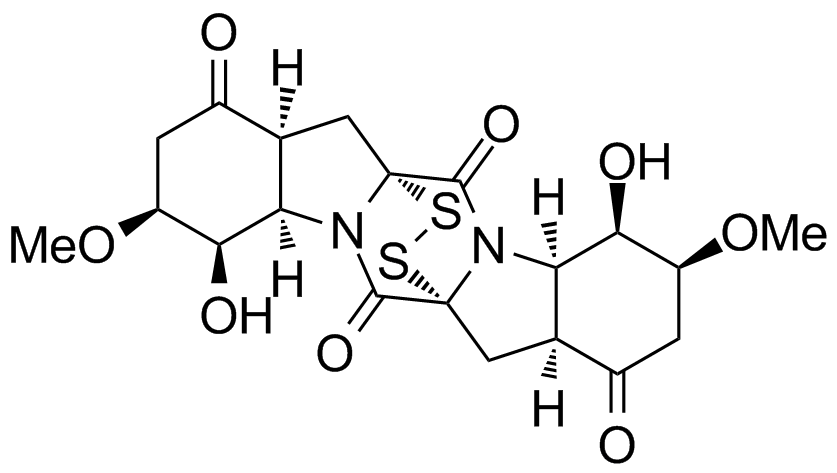
Rostratin C
Die Rostratine A–D gehören zur Substanzklasse der Mykotoxine. Die marinen Naturstoffe mit dem Epithiodiketopiperazin-Gerüst wurden 1997 bei Hawaii aus dem Pilz Exerohilum rostratum isoliert. 2004 konnten die Strukturen aller vier Sekundärmetaboliten aufgeklärt werden. Ihre in vitro Cytotoxizität gegen das menschliche Darmkarzinom der Zellline HCT-116 machen sie als neue Leitstrukturen für die Naturstoffsynthese interessant.
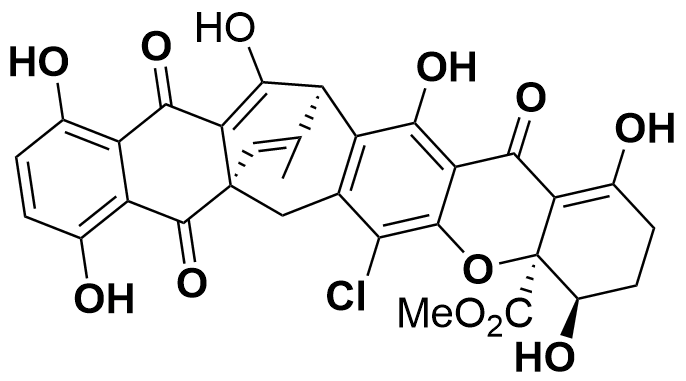
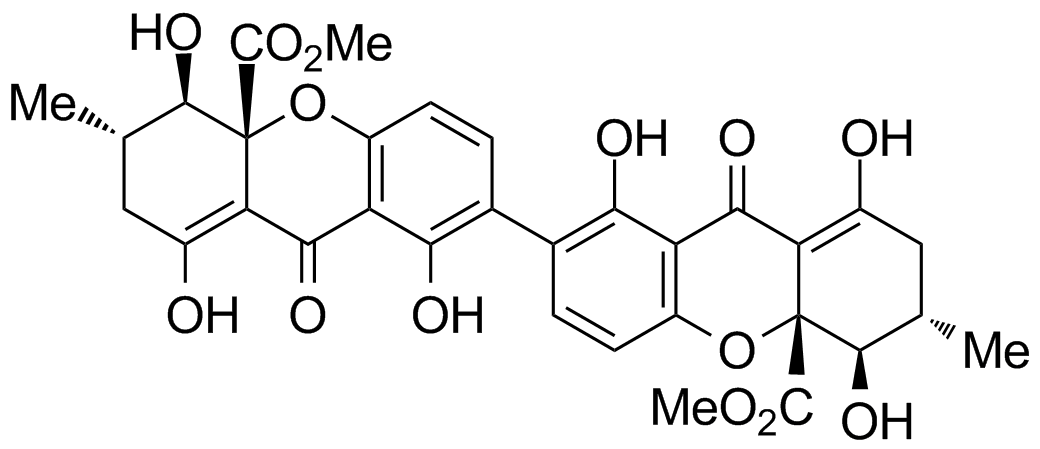
Secalonsäure D
Die Secalonsäuren A-G wurden erstmals aus dem Schlauchpilz Claviceps purpurea („Mutterkorn“) isoliert und zeigen vielfältige biologische Aktivität, z. B. Cytotoxizität und antibakterielle Eigenschaften. Sie wurden vor mehr als 100 Jahren entdeckt; dennoch wurde bis heute keine Totalsynthese dieser Verbindungs-klasse erreicht.
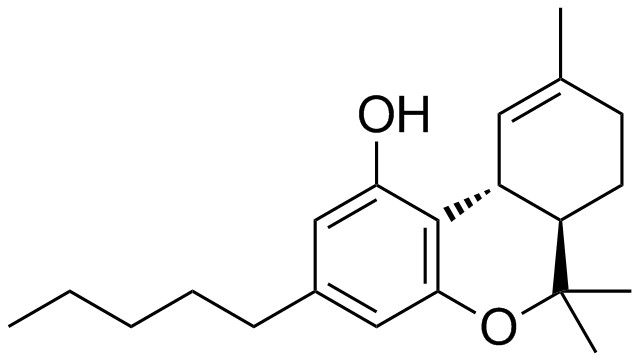
Spiculoinsäure A
Im Jahr 2004 wurde der bis dahin unbekannte polyketidische Naturstoff Spiculoinsäure A von Andersen et al. aus dem karibischen Schwann Plakortis angulispiculatus (Carter) isoliert. Die Struktur und relative Stereochemie des hochsubstituierten Hydrindanes wurde durch eine Kombination von massenspektroskopischen und NMR-Untersuchungen erreicht. Darüber hinaus weist die Substanz cytotoxische Aktivität gegenüber der menschlichen Brustkrebszelllinie MCF-7 auf (IC50 8 µg/ml), was diese Substanz zu einem interessanten Kandidaten für die Wirkstoffentwicklung macht.
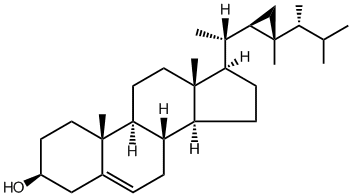
Gorgosterol
Gorgosterol und eine Vielzahl anderer Sterole werden von Dinoflagellaten produziert, einschließlich derer der Gattung Symbiodinium, den obligaten intrazellulären Symbionten von riffbildenden Korallen. Bis heute sind die biologischen Funktionen von Gorgosterol und anderen Sterolen in dieser Symbiose unbekannt; wir stellen die Hypothese auf, dass sie vom Symbionten auf den Korallenwirt übertragen werden, wo sie möglicherweise eine wichtige Rolle im Lipidstoffwechsel oder bei der Steroid-Signalübertragung spielen. Unser Ziel ist es, Gorgosterol zu synthetisieren, möglicherweise auch mit Modifikationen, um seine biologischen Funktionen in der Symbiose anhand der marinen Seeanemone Aiptasia, einem aufstrebenden Modellsystem für Korallen, zu bewerten.
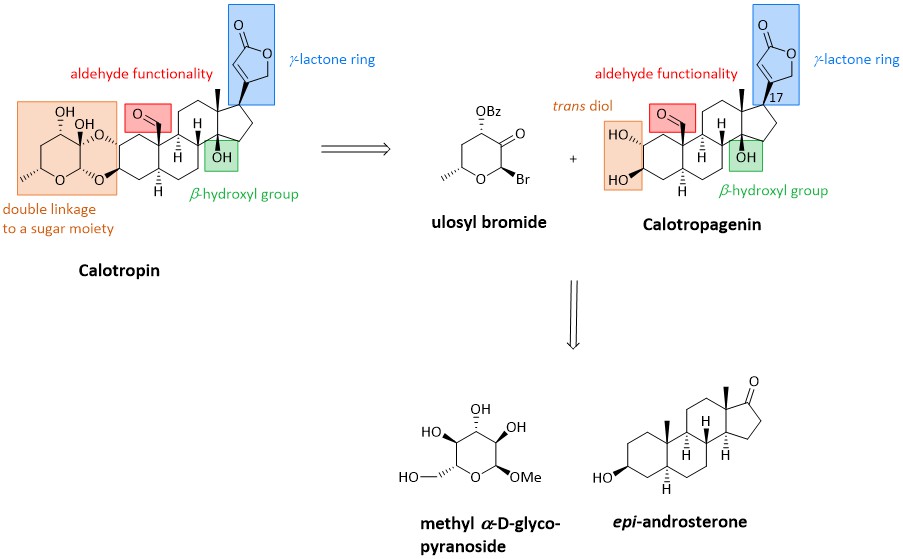
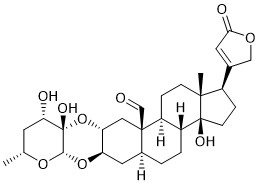
Calotropin
Das natürlich vorkommende Steroid Calotropin gehört zur Klasse der Herzglykoside, die seit über 200 Jahren als Therapeutika zur Behandlung von kongestiver Herzinsuffizienz eingesetzt werden. In den letzten Jahren wurde ihre aufkommende Rolle als potentielle Anti-Krebs-Wirkstoffe entdeckt. Insbesondere Calotropin wurde als Inhibitor des Wnt-Signalweges identifiziert. Dieser Signalweg reguliert eine Reihe wichtiger zellulärer Prozesse, darunter die Embryonalentwicklung, Zelldifferenzierung und -proliferation, und kann auch mit verschiedenen menschlichen Krankheiten in Verbindung gebracht werden. So sind beispielsweise 80 % der Fälle von Dickdarmkrebs auf einen aberranten aktiven Wnt-Signalweg zurückzuführen. Inhibitoren dieses Signalweges, wie Calotropin, könnten daher als Leitstrukturen für neue Therapeutika bei Wnt-Signal-abhängigem Krebs dienen. Nicht nur die interessanten biologischen Eigenschaften, sondern auch die synthetisch anspruchsvolle Struktur von Calotropin haben uns motiviert, eine Strategie für seine Semisynthese ausgehend von leicht verfügbaren Ausgangsmaterialien wie Methyl-α-D-glucopyranosid und Epi-Androsteron zu entwickeln. Für die Synthese des Ulosylbromids wird eine aus der Literatur bekannte Strategie verfolgt, während die Synthese von Calotropagenin ausgehend von Epi-Androsteron die folgenden Aspekte umfasst:
- Oxidation von C-2 und C-19, um die Einführung des trans-2α,3b-Diol-Strukturmotivs und der Aldehydfunktionalität zu ermöglichen
- Diastereoselektive Einführung der b-Hydroxylgruppe unter Inversion des vorliegenden stereogenen Zentrums
- Einführung des γ-Butenolidrings an C-17